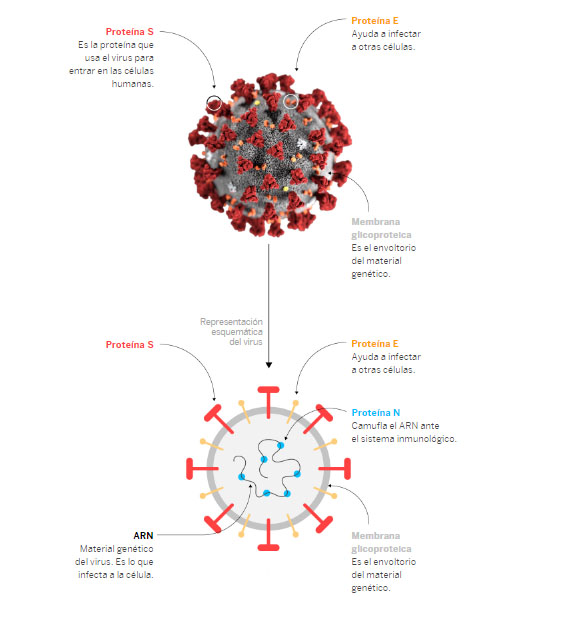
El coronavirus SARS-CoV-2 produce en humanos la enfermedad conocida como COVID-19, es un virus RNA de cadena sencilla, que accede a células de nuestro organismo a través de la interacción de la proteína de espiga S (S: spike protein) presente en la superficie del virus, con un receptor celular humano ACE2 (angiotensin-converting enzyme-2: ACE2, siglas en inglés) presente en la superficie de células de la mucosa, pulmones, etc., una vez dentro de la célula del hospedador, se inicia la replicación del material genético del virus (RNA) y la producción de nuevas partículas virales. La propagación de la enfermedad ha sido tan rápida a nivel mundial que se ha convertido en un problema de salud pública, lo cual ha traído como consecuencia que la Organización Mundial de la Salud (OMS) haya declarado la enfermedad como una pandemia mundial global, lo cual a su vez ha generado la necesidad inmediata de desarrollar métodos de detección del virus de gran precisión, rápidos y rentable. Impresionante ha sido el impacto científico que ha tenido el estudio de este nuevo virus, generando una gran cantidad de información a través de publicaciones científicas y ciencia abierta.1
La identificación del SARS-CoV-2 en pacientes que presentan la enfermedad, puede llevarse a cabo a través de técnicas moleculares asociadas a su material genético, o mediante aproximaciones inmunológicas. La prueba molecular que se ha utilizado con mayor sensibilidad y confiabilidad, y considerada como la prueba de oro, es una variante de la reacción de PCR estándar llamada PCR en tiempo real (Real-Time PCR: RT-PCR, siglas en inglés) que incluye la enzima transcriptasa inversa cuya función es llevar a cabo la síntesis de DNA a partir del material genético viral (RNA). Las muestras utilizadas para llevar a cabo dicha prueba provienen de secreciones respiratorias como exudados nasofaríngeos u otras muestras del tracto respiratorio superior, incluyendo hisopados de garganta, esputo y saliva.2
Varios son los blancos genéticos del virus que pueden amplificarse de forma específica, por ej. secuencias del genoma viral que generan la proteína de espiga (S), marco abierto de lectura 1ab (open reading frame: ORF1ab. Siglas en inglés), o la nucleocápsida N, entre otros. Este último es utilizado para la prueba CDC 2019-nCoV Real-Time RT-PCR Diagnostic Panel.3,4,5
Aunque la RT-PCR es una técnica de alta sensibilidad y especificidad, algunas limitaciones han sido indicadas, entre ellas se incluyen las siguientes: a. se requiere de equipo y personal especializado para llevarla a cabo; b. requiere al menos 3-4 horas para obtener resultados; y c. la toma y manipulación de la muestra a analizar es importante, dado que un mal manejo de la misma puede generar falsos positivos al igual que falsos negativos. Debido a lo anterior, la búsqueda de nuevos métodos alternativos para el diagnóstico temprano y preciso del SARS-CoV-2 es una necesidad. Algunos de estos nuevos métodos están combinados con la técnica de edición genética llamada CRISPR.
Uno de estos nuevos ensayos, llamado SARS-CoV-2 DNA Endonuclease-Targeted Trans Reporter CRISPR (DETECTR), está basado en la técnica de edición genética CRISPR-Cas129-13 para la detección de SARS-CoV-2, a partir de RNA de muestras extraídas de paciente. En dicho ensayo, los autores llevan a cabo en forma simultánea la transcripción inversa del RNA y la amplificación de la hebra de DNA obtenida, mediante una reacción de PCR isotérmica (RT-LAMP: Loop-Mediated Isothermal Amplification Method).6,7
Los cebadores de la reacción de amplificación LAMP fueron diseñados, y modificados para la amplificación de los genes E (envoltura) y N (nucleoproteína) del SARS-CoV-2, de manera similar a aquellos utilizados por el ensayo RT-PCR de la OMS y del CDC de EE. UU. El siguiente paso fue el diseño de los RNA guías (gRNA) para direccionar la acción de la nucleasa Cas12 y detectar en forma diferencial los coronavirus de tipo SARS: a. SARS-CoV-2 (acceso NC_045512); b. coronavirus de tipo SARS murciélago (bat-SL-CoVZC45, acceso MG772933); y c. SARSCoV (acceso NC_004718), en el gen E y específicamente detectar solo SARS-CoV-2 en el gen N. Los resultados mostraron que la detección basada en CRISPR-Cas12 puede distinguir SARS-CoV-2 sin reactividad cruzada para las cepas de coronavirus relacionadas utilizando gRNA del gen N y con reactividad cruzada esperada para el gRNA del gen E. El ensayo DETECTR puede ejecutarse en aproximadamente 30-40 min y el resultado puede visualizarse en una tira de flujo lateral a través de un marcador reportero como biotina luego de amplificación y acción del sistema Cas12-gRNA.6
Cuando se comparó el límite analítico de detección (LoD) del ensayo fluorescente RT-LAMP / Cas12 DETECTR en relación con el ensayo de RT-PCR-CDC aprobado por el Departamento de Salud Pública, EUA. para la detección de SARS-CoV-2, se muestra que la LoD estimad para este último es de 1 copia por microlitros de reacción, lo que es consistente con el rendimiento analítico en el prospecto de la FDA de EE. UU., frente a 10 copias por microlitros de reacción para el ensayo DETECTR. Por otro lado, el ensayo DETECTR ofrece una alternativa visual más rápida respecto al ensayo de RT-PCR para SARS-CoV-2 de los Centros para el Control y la Prevención de Enfermedades de EE. UU., con una lectura cualitativa de fácil interpretación, con una predicción positiva del 95% luego de un estudio comparativo de 83 muestras del tracto respiratorio de pacientes afectados de la enfermedad.
La combinación de la amplificación isotérmica con la tecnología CRISPR-Cas12 en el ensayo DETECTR, mostró una serie de ventajas importantes, entre las cuales tenemos: a. se desarrolla una prueba rápida para la detección de SARS-CoV-2 en muestras clínicas (30-40 min), con una precisión comparable a la qRT-PCR; b. no existe la necesidad de un equipo de PCR (termociclador); y c. tal como lo indican los autores, el ensayo podría permitir pruebas en puntos de atención fuera del laboratorio de diagnóstico clínico, como aeropuertos, departamentos de emergencia locales y clínicas y otros lugares.
Dicho ensayo ha sido validado en muestras de referencia artificiales y muestras clínicas de pacientes en los Estados Unidos. La validación clínica de este ensayo en respuesta al reciente borrador de orientación de la FDA de EE.UU., está en curso.
Referencias
- Galocha A. & Domínguez N. (2020). Así infecta el Coronavirus. https://elpais.com/elpais/2020/03/06/ciencia/1583515780_532983.html
- Intra Med (2020) Interpretación de pruebas diagnósticas. doi:10.1128/JCM.00557-20. 2. https://www.intramed.net/contenidover.asp?contenidoid=96110&pagina=1
- Rubén Megía González 2020 https://genotipia.com/sars-cov-2-pcr/.
- CDC 2019-Novel Coronavirus (2019-nCoV) Real-Time RT-PCR Diagnostic Panel https://www.fda.gov/media/134922/download
- SINC (2020). Así son las pruebas de PCR que se utilizan para detector el coronavirus. https://www.agenciasinc.es/Noticias/Asi-son-las-pruebas-PCR-que-se-utilizan-para-detectar-el-coronavirus
- Broughton, J.P.et al. (2020). Nat Biotechnol https://doi.org/10.1038/s41587-020-0513-4. https://www.nature.com/articles/s41587-020-0513-4
- Mendoza-León A. (2010). Diagnóstico Molecular de Enfermedades Infecciosas: Loop-Mediated Isothermal Amplification (LAMP) Method. https://piel-l.org/blog/18238
Imagen tomada de Así infecta el coronavirus, El País España https://elpais.com/elpais/2020/03/06/ciencia/1583515780_532983.html?ssm=TW_CC a través de @materia_ciencia
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998


Alexis gracias por este articulo. Las autoridades sanitarias de los diversos paises deberian entenderlo para no comprar pruebas ineficientes. Gracias
Allí la importancia de un trabajo en conjunto entre estado y desarrollo científico desde todo punto de vista. Una de las grandes lecciones de la pandemia ha sido la importancia en la inversión de ciencia y tecnología, y el papel que juega la ciencia en un país, y la importancia de su opinión
Allí la importancia de un trabajo en conjunto entre estado y desarrollo científico desde todo punto de vista. Una de las grandes lecciones de la pandemia ha sido la importancia en la inversión de ciencia y tecnología, y el papel que juega la ciencia en un país, la importancia de su opinión
Gracias profe. muy interesante.
Respuesta a Maria A. Vethencourt Ysea: Una respuesta al diagnóstico temprano del SARS-CoV-2, aunque no es la única metodología que involucra el sistema CRISPR, pero es una proyección importante de la aplicabilidad de la edición genética.