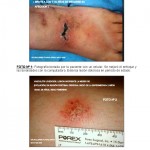
Apreciados amigos: Les envío un caso de vasculitis livedoide visto recientemente que creo que puede ser de interés a los lectores, por una serie de alteraciones vasculares relacionado con sustancias mucinosas que no había observado en casos anteriores
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998





Estimado Dr. Planas Giron:
Lo felicito por la excelente presentación iconográfica del caso.
Realmente las imágenes clinicas llevan a la sospecha de vasculitis livedoide. Sin embargo la histopatología -tal como Ud. lo plantea- es diferente a lo esperado. Existen elementos histopatológicos que «sobran» para este caso. Me permito sugerir que se realice un seguimiento clínico e inmunológico estricto de la paciente.
Supongo que Ud me permitirá pensar en voz alta… Cabe recordar que dentro de las mucinosis secundarias están las enfermedades del colágeno -lupus?-
Sería muy interesante que en el futuro pudiera comentarnos la evolución del caso.
Cordialmente
Dra. Maria Bibiana Leroux
Efectivamente Dra. Leroux. En el caso anterior de vasculitis livedoide (VL) que presentamos meses atrás en este interesante Blog, no observé este componente mucinoso tan importante, que me ha llevado a plantear la hipótesis de que probablemente en esta paciente su cuadro de vasculopatía esté asociada a una colagenosis de fondo, como efectivamente Ud. lo señala (Lupus Eritematoso). Si se tiene en cuenta que en muchos casos de LES los autoanticuerpos se desarrollan muchos meses o años antes de la presentación de síntomas de LES., es razonable plantear tal hipòtesis.
Se ha reportado cuadros de VL asociada a enfermedades autoinmunes como el S. Sjögren (Cardoso R, Goncalo M, Tellechea O, et al. Livedoide vasculopathy and hipercoagulability in a patient with primary Sjögren´s syndrome. Int J Dermatol 2007; 46:421-4). Igualmente la asociación con sindrome antifosfolípidos y poliarteritis nodosa se ha reportado igualmente.
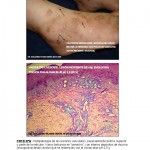
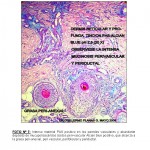
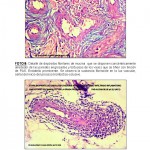
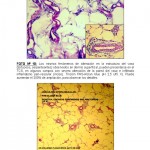
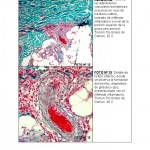
Si Ud. analiza, la morfología y disposición de los vasos, en la dermis profunda, media y superficial, observará que los cambios experimentados por el paquete vascular, tanto superficial como profundo, corresponden a la clásica VL, ( vasos tortuosos en figuras de «penacho») libres en el sector superficial de infiltrado inflamatorio. En dermis profunda y TCS, los vasos parecieran que estuvieran atacados por un severo y denso infiltrado linfocitario, con diapédesis de eritrocitos, y los fenómenos de coagulopatía, cambios que se pueden observar en las lesiones tempranas de VL, pero el factor mucinoso es el que me llama la atención. Creo que hay que profundizar en este aspecto para descartar un componente de enfermedad del tejido conjuntivo asociado.
Agradecido Dra. Leroux por su intervención. Espero que continuemos en este interesante intercambio de opiniones.
Un saludo cordial
Dr. Guillermo Planas Girón
Caracas-Venezuela
GUillermo, cuando observo la pulcritud , la impecabilidad de tus presentaciones, la claridad mental con que razonas y discutes, entiendo una vez más, por que hay docentes de docentes. Excelente caso, Excelente asociación , además de estimulante!!!
GRacias Guillermo!
Estimado Guillermo:
Muy interesante caso, muy demostrativo con excelente fotos clínicas e HP de Atrophie blanche o vasculopatía livedoide.
Extraña patología vasculítica que vemos más frecuentemente en mujeres en las piernas como demuestras en el ilustrativo caso.
La AB o VL es sobretodo un signo resultante de muchas patologías. me parece interesante el planteamiento q por la mucinosis intensa existente esta vasculitis podría asociarse en un futuro a colagenopatías tipo LE.
es importante descartar sobretodo en mujeres jóvenes (posibilidad de pérdidas fetales recurrentes o ACV trombóticos) la asociación con sindrome antifosfolípido (ACA IgG e IgM, VDRL, anticoagulante lúpico) además de repetir periódicamente su perfil seroinmunológico.
siempre la antiagragación plaquetaria: ASA o clopidogrel o la pentoxifilina (probablemente la efectividad dependa de la dosis) serían de utilidad. incluso en algunos pacientes sería necesaria la anticoagulación.
usar antinflamatorios por tiempos cortos ayuda en la vasculitis y en disminuir la molestia.
Gracias nuevamente Guillermo por demostrativo caso y oportunidad de opinar en tan prestigioso foro.
Ricardo Pérez Alfonzo
Buenas noches:
Excelente presentación clínica e hisopatológicamente.
La Atrofia Blanca o Vasculopatía Liveloide (esta última denominación, es tal vez la más apropiada, ya que no hay una verdadera vasculitis) no es tan infrecuente, yo he visto un número importante de casos en mi consultorio médico; en la mayoría de ellos hay un antecedente franco de Insuficiencia venosa crónica con manifestaciones clínica de Dermatitis de Estasis, en donde encontramos lesiones cicatrízales secundarias al estasis venoso. También podemos encontrar este mismo aspecto clínico en Vasculitis leucocitoclastica y secundarias a enfermedades del colágenos como Lupos eritematoso y Esclerodermia principalmente.
En los pacientes con claros antecedentes de insuficiencia venosa crónica hay un flujo venosos retrogrado, que lleva a un aumento de la presión venosa y a un continuo aumento de la presión capilar, con dilatación de los capilares y esto lleva a salida o escape de fibrina del compartimiento intravascular con formación de manguitos de fibrina alrededor de los vasos, constituyendo esto una franca barrera para la permeación de oxigeno y nutrientes al tejido circundante. Esta dilatación conlleva a una franca disminución de la velocidad del flujo capilar, adhesión de leucocitos induciendo la liberación de enzimas proteolíticas y metabolitos superóxidos, causando destrucción de tejido (ulceración): El estasis local re-alimenta éste proceso de adhesión de leucocitos; hay disturbios entre los factores pro-coagulantes y anticoagulantes, más el estasis, determinan coagulación intravascular local o sectorial. La oclusión vascular disminuye la tensión del oxigeno en los tejidos, llevando a fibrosis y a oclusión de los capilares en la dermis y la aparición del aspecto clínico morfológico de la atrofia blanca de Millian. El tarumá mínimo o trivial (como rascado) determina la aparición de ulceración; la Atrofia blanca puede surgir después de las ulceraciones o antes.
La presencia de Atrofia Blanca sin insuficiencia venosa crónica, también sugiere comprometimiento local de desordenes de la coagulación, como el síndrome de anticuerpos antifosfolipidos, la cual pudiera ser mediado por estados de activación palquetaria y/o un estado de hipercoagulación primaria o secundaria a otros factores como la deficiencia de la Proteína C y anormalidades fibrinolíticas, además de la presencia de los anticuerpos antifosfolípidos.
En la discusión de otros casos en este mismo blog, hemos escuchado insistentemente de parte de destacados dermopatologos la importancia de la presencia de mucina en el tejido, lo cual habla a favor de colagenopatía (Lupos) de manera que debemos insistir en las pruebas inmunológicas, recordemos que las enfermedades del colágenos son evolutivas, de esta forma , que es imperativo repetir las mismas.
En relación al tratamiento , comento los siguiente:
Hemos utilizado la Ciclosporina (3-5 mg/kg/dia con excelentes respuesta, solo que al suspenderla la recaída es la regla.
También hemos usado pentoxifilina a dosis alta 600 mg tid, cuando la toleran, los resultados a largo plazo es buena.
Nuevamente quiero felicitar a Guillermo Planas Girón por tan excelente material y agradecer que haya utilizado PIEL-L LATINOAMERICANA para su difusión.
Rolando Hernández Pérez
Barinas/Venezuela
Quiero agradecer a los distinguidos colegas que han intervenido con sus palabras de estímulo y sus interesantes aportes dirigidos al esclarecimiento y al mejor conocimiento y manejo de esta arteriopatía de carácter recidivante, la cual en ocasiones se asocia a enfermedades autoinmunes.
Su frecuencia puede ser discutible. En USA (2008) se considera a la VL un desorden infrecuente e internacionalmente la condición es incomún en todo el mundo. También cabe la posibilidad del sub-registro por potenciales confusiones con otros cuadros vasculíticos, incluyendo úlceras de éstasis.
Independientemente de las interesantes concepciones fisiopatológicas y patogénicas que pudiesen variar si el cuadro está asociado o no a livedo reticularis y/o a procesos varicosos-flebíticos, como se ha reportado en la literatura, lo cierto es que la VL es de difícil tratamiento.
De acuerdo a una actualización reciente de Scheinfeld NS en eMedicine Dermatology (17 de Marzo de 2008), los especialistas -en tanto descartan enfermedades asociadas- pueden ofrecer a los pacientes una serie de recursos terapéuticos, que lamentablemente no son efectivos en todos los casos.
1) Pentoxifilina (Trental (R): 400 mg t.i.d. Se piensa que aumenta el flujo sanguíneo en los capilares, a través de su acción sobre los GR que se tornan más flexibles, reduciendo su viscosidad, como nos los expuso en el interesante análisis recientemente publicado por la Dra. Leroux en su módulo de Colagenopatía al día. En el caso presentado no se ha obtenido mayores beneficios a dosis de 800 mg/día. Es posible, en caso de tolerarlo, aumentar la dosis a 1.200 mg/día por más de 3 meses. o asociarlo como sugiere Ricardo, al Copridogrel o a la aspirina.
2) Heparina de bajo peso molecular (LMWH), sugerido por Hairston et al (2003).
3) Yang et al (2003) y Juan WH et al (2006), reportan mejorías extraordinarias con el oxígeno hiperbárico.
4) Dipyridamole (Persantin) (75 mg q.i.d)+ 325 mg. de aspririna /diaria x 3-6 semanas), aunque se han reportado iguales resultados con dosis menores de Dipyridamole (50 mg. t..i.d) + la misma dosis de aspirina mencionada.
5) Nifedipine (Procardia): 20 mg t.i.d: impide el depósito de fibrina, unos de los pasos iniciales de la patogenia, aumentando la perfusión en vasos superficiales.
6) Otras alternativas terapéuticas, incluyendo el uso de la inmunoglobulina IV (Amital H, Levy Y, Shoenfeld , 2000), que aunque Scheinfeld , lo considera terapias experimentales, ha habido buena experiencia en el HUV (UCV).
Si el tiempo nos los permite, y antes de que concluya la presente edición el Viernes, me gustaría oir experiencias y opiniones con el uso de estas diversas modalidades terapeúticas.
Un saludo cordial,
Dr. Guillermo Planas Girón
Caracas-Venezuela
Estimados colegas les informo que cuando necesiten utilizar Clopidogrel como antiagregante plaquetario nunca lo combinen con inhibidores de bomba de protones (omeprazol, lansoprazol, esomeprazol, pantoprazol, rabeprazol).
Recientemente se publicó una nueva interacción entres estos y el clopidogrel, la combinación reduce el efecto antiagregante y falta de eficiacia como antiaterotrombótico (Sibbing D, et al. Impact of proton pump inhibitors on the antiplatelet effects of clopidogrel. Thromb Haemost 2009; 101:714-719).
Si necesitan usar protectores gastrointestinales y clopidogrel usen antiH2.
Saludos cordiales
Juan Antonio Chassaigne
Gracias Juan Antonio por tu importante advertencia sobre el uso de inhibidores de la bomba de protones (omeprazol, esomeprazol, etc) conjuntamente con la terapia de clopidrogel (Plavix de 75 mg (R) Cravic (R), etc), indicados como antiagregantes plaquetarios.
Es bueno que nos los hayas refrescado con literatura más reciente, porque ya el año pasado, se publicaron importantes trabajos previniendo el uso de estas drogas en forma simultánea, produciendo una disminución importante del efecto antiplaquetario del clopidrogrel en sindromes coronarios inestables.
A estos factores se agrega que se ha demostrado que existen factores genéticos que regulan la efectividad de la droga en sus funciones antiplaquetarias, es decir que hay pacientes portadores de alelos específicos como CYP2C19 que causan pérdida de la función antiplaquetaria de la droga, demostrable en aquellos pacientes receptores de stent coronario y en IM. Pero este no es mi campo de acción, solo quería mencionarte que hay otro producto denominado «prasugrel «, otro inhibidor P2Y, que parece no ser afectado por la isoenzima mencionada ni tiene interferencia con el Omeprazol y drogas similares, pero que aún no ha sido aprobado por la FDA.
Así como se puso de moda la indicación del clopidrogrel como antiagregante plaquetario (He observado que aproximadamente un 90% de mis pacientes mayores de 60 años, portadores de alguna cardiopatía o secuelas de ACV, ingieren la droga. La competencia con la Cor-aspirina (R) es bestial. Hay pacientes a quienes les indican ambas drogas) , no te extrañe que el próximo que sustituya al clopidrogrel, sea el «prasugrel». Y quien puede presagiar que esta última presentación, no sea de un beneficio importante para los pacientes que sufren VL, el tema que nos ocupa.
Ref.
1) Freedman JE and Hylex EM. Clopidrogel, Genetics, and Drug Responsiveness. N England J Med 360;4:411-413 January 22, 2009
2) Gilard, et al. Influence of omeprazole on the antiplatelet action of clopidrogrel associated with aspirin: the randomized, double-blind OCLA(Omeprazole Clopidrogrel Aspirin) study. J Am Coll Cardiol 2008;51:256-60
Un saludo cordial
Dr. Guillermo Planas Girón
Ccs-Venezuela.
Estimado Dr. Planas: En esta edición, en la sección de Comunicaciones Importantes está el Comunicado de la Agencia Española de Medicamentos de fecha 03 de Junio de 2009, precisamente sobre la interacción de Clopidogrel y los IBP. Se menciona lo del polimorfismo genético y la existencia de pacientes que son metabolizadores lentos de clopidogrel.
Saludos
Juan Antonio