La situación actual con respecto a la expansión de resistencia antimicrobiana a antibióticos y otras drogas de uso medicinal, es profundamente preocupante en términos de salud pública. Algunos de los muchos microbios resistentes incluyen Enterobacteriaceae resistente al carbapene, Enterobacteriaceae productoras de ?- lactamasa de espectro extendido, Enterococcus resistente a la vancomicina, Staphylococcus aureus resistente a la meticilina y tuberculosis resistente a múltiples fármacos. El conocimiento de la evolución, diseminación y expresión genética asociada a esta resistencia, es de vital importancia en la toma de decisiones que puedan establecer límites a la expansión del problema.1,2
A objeto de evitar un colapso globalizado y evitar fallas críticas en nuestra capacidad para controlar infecciones generadas por microorganismos resistentes, se hace necesario la identificación de nuevos blancos y nuevas drogas al igual que aprovechar las tecnologías emergentes para generar soluciones alternativas.
Esto ha generado un gran interés en las aplicaciones de fagos antimicrobianos, como por ejemplo el uso terapéutico de virus lisogénicos contra infecciones bacterianas donde el sistema inmunológico jugaría un papel fundamental en el éxito de tal terapia.2,3,4 Estos virus llamados también bacteriófagos, a diferencia de virus que producen lisis bacteriana, incorporan su material genético al genoma bacteriano (profago) y se multiplican en sincronía con la bacteria sin causar muerte bacteriana.
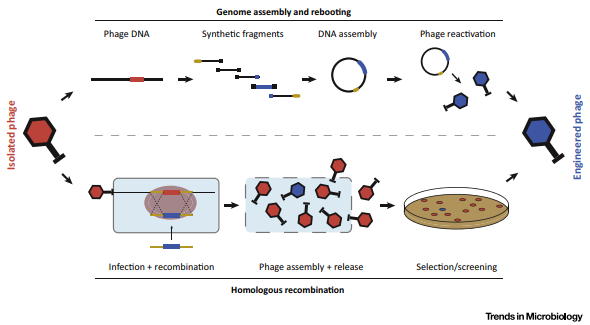
La eficacia de los antibióticos existentes se ha visto comprometida por la evolución generalizada de la resistencia en bacterias patógenas. La propagación epidémica de la resistencia se puede detener al prevenir la evolución de la resistencia dentro de los hospederos o la transmisión entre los hospederos. En este sentido, las nuevas tecnologías han puesto en evidencia el potencial uso de terapias virales; es así como se han propuesto varios enfoques para tratar de abordar la resistencia a los antimicrobianos, utilizando fagos. Avances en biología sintética han hecho posible, por ejemplo, diseñar fagos lisogénicos para suministrar redes genéticas sintéticas que interfieran con importantes procesos intracelulares bacterianos con el objetivo de causar la muerte celular bacteriana o re-sensibilizar las bacterias a los antibióticos o revertir la resistencia a antibiótico.
Ahora es el momento de pasar del desarrollo de técnicas al desarrollo de conceptos de ingeniería que proporcionan un valor agregado deseado a un fago determinado para su uso seguro en una terapia viral.
Referencias
1. Mendoza-León 2013. Resistencia microbiana: ¿a qué se debe esto? https://piel-l.org/blog/33340
2. Teitzel G. 2019. Responding to Antimicrobial Resistance with Novel Therapeutics. Trends in Microbiology, 27(4). https://doi.org/10.1016/j.tim.2019.01.007
3. Monteiro R. et al. 2018. Phage Therapy: Going Temperate?. Trends in Microbiology. https://doi.org/10.1016/j.tim.2018.10.008
4. Kilcher S. and Loessner M.J. 2018. Engineering Bacteriophages as Versatile Biologics. Trends in Microbiology. https://doi.org/10.1016/j.tim.2018.09.006
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998

Gracias profesor Mendoza, estos fagos serian una especie de nuevos probioticos, incorporandose a los guerreros desplazadores de los malos guerreros antisalud. El concepto, de la nueva esencia de la terapia medica, desplazar y no guerrear. Gracias
Jaime Piquero Martin
Buen comentario Jaime. A la fecha hay adelantos promisorios del uso de virus en terapia genética; sin embargo, entre los problemas a resolver esta el control de expresiones adversas por parte de estos virus. Los virus forman parte del futuro de la terapia genética