Hipersensibilidad a Medicamentos o Reacciones Adversas a drogas. Que está pasando con la inmunopatogénesis de la alergia a medicamentos mediada por células T
Las reacciones adversas a medicamentos juegan un importante papel en los pacientes por su alta morbilidad y mortalidad, un porcentaje importante de ellas pueden ser prevenibles.
Actualmente se conoce que estas reacciones son producidas por efectos farmacológicos de la droga tales como aquellas que vemos en pacientes con el síndrome de activación de mastocitos a causa de una droga lo cual no es mediado por IgE. O bien son reacciones mediadas inmunológicamente. Estas comprenden un grupo de variado de entidades clínicas y pueden ser mediadas por células B y anticuerpos (Tipos I, II y III de la clasificación de Gell y Coombs) o las mediadas por células T (Tipo IV de la clasificación de Gell y Coombs)
Cuando son mediadas por IgE corresponden a la típica reacción alérgica. Sin embargo, estas no son las más frecuentes y recientemente se han establecido otros mecanismos inmunológicos de gran interés e importancia. En esta sección nos ocuparemos de las reacciones a drogas mediadas por células T.
En la revisión de White y colaboradores (2015), se afirma que 50% de estas reacciones son prevenibles. Son predecibles debido a la conocida acción farmacológica de la droga en su blanco. Alrededor del 20% no se pueden anticipar basándose en principios farmacológicos solamente y se les denominaban anteriormente idiopáticas o no predecibles.
Entre las reacciones a drogas mediadas por células T y clínicamente relevantes se han incluido las siguientes formas clínicas exantema retardado sin síntomas sistémicos (erupción maculo papular), dermatitis de contacto, reacción con eosinofilia y síntomas sistémicos (DRESS), síndrome de Steven- Johnson (S/J), necrolisis epidérmica tóxica (TEN), pustulosis exantemática aguda, erupción fija medicamentosa y patologías específicas a un solo órgano tales como afecciones hepáticas o pancreatitis.
Variaciones alélicas de los genes que codifican para proteínas del sistema mayor de histocompatibilidad (MHC) se pueden asociar muy cercanamente a estas reacciones adversas, de manera que la genética del individuo juega un papel muy importante. Se conocen poblaciones susceptibles con riesgo a presentar reacciones a drogas mediadas por células T.
Es conveniente recordar las características de las células T que intervienen en este tipo de reacciones. Durante el desarrollo de las células en el timo se presentan una serie de procesos de selección para generar un repertorio funcional específico. El receptor de células T (TCR) codifica el repertorio de HLA. La unión del TCR con el péptido ligando del complejo mayor de histocompatibilidad (MHC) produce una proliferación clonal que resulta en la diferenciación de células T efectoras o de memoria. Las células T memoria expresan el marcador CD45RO y carecen del receptor CCR7 que es el receptor de anidación en ganglios linfáticos. Así, ese grupo celular tiene la facultad de migrar a los tejidos y alojarse en los tejidos de contacto y de fácil re exposición con el agente patógeno.
Allí liberan citoquinas pro inflamatorias (TNF ?, IL2, INF ?) y péptidos citotóxicos iniciándose la respuesta inmune al contacto con el antígeno. El contacto de las células T con el MHC se realiza mediante la cadena de polipéptidos ?? del TCR. Estos receptores están compuestos por regiones variables que son las que aportan la variabilidad del TCR y permiten el reconocimiento de gran cantidad de patógenos produciéndose la respuesta inmune.
Los individuos heterocigotos en los locus HLA expresarán más diversidad en las proteínas MHC lo que confiere reconocimiento e inmunidad a un mayor número de patógenos.
Aunque ha sido demostrado firmemente la mediación de células T para las reacciones adversas a drogas los mecanismos moleculares de estas reacciones no se conocen totalmente. Sin embargo, existen numerosos reportes que asocian HLA alelos con las reacciones de hipersensibilidad a drogas
El papel de la respuesta inmune mediada por células T ha sido firmemente establecido. Sin embargo, los mecanismos moleculares específicos en que se basan estas reacciones no son bien conocidos. Existen múltiples publicaciones que reportan la asociación de reacciones adversas a drogas y alelos de HLA (White et al., 2014 y Pavlos et al., 2015).
Se han descrito tres modelos no excluyentes que describen como una pequeña molécula farmacológica puede inducir la reactividad de células T, estos son: el modelo hapteno/prohapteno. La droga o su metabolito se une por un enlace covalente a una proteína endógena que por un procesamiento intracelular genera péptidos modificados que son reconocidos como extraños en el MHC e inducen una respuesta inmune mediada por células T. Ejemplos incluyen la unión de derivados de la penicilina a albúmina sérica y modificación de proteínas por el metabolito sulfametoxazole (Naisbit et al., 2001 y Padovan et al., 1996).
El segundo modelo de la interacción farmacológica se ha denominado modelo p-i En este modelo p-i, es decir de interacción farmacológica la droga productora de la reacción se uniría por un enlace no-covalente o bien al receptor de células T (TCR) o a proteínas del MHC de una manera independiente de péptidos y directamente activaría a células T. Algunos trabajos han demostrado que hay drogas capaces de inducir respuestas T en la ausencia de procesamiento intracelular de péptidos, después de la fijación a células presentadoras de antígenos. Se ha observado que se puede producir activación de células T in vitro minutos después de la exposición a la droga (Pichler et al., 2006).
El tercer modelo es el de repertorio alterado de péptidos. Se producen péptidos modificados cuando la droga ocupa una posición en el péptido de unión con el MHC y cambia su estructura química, estos péptidos modificados serán reconocidos como extraños y por lo tanto se induce una respuesta inmunológica mediada por células T.
Citaremos como ejemplos, algunas drogas que han sido estudiadas con más profundidad. Entre ellas están abacavir, carbamazepina, allopurinol, dapsona, sulfametoxasol, amoxicilina clavulanico, diclofenac y oxcarbazepina. Estudios recientes han permitido conocer algunos de los diferentes síndromes que pueden producir estos medicamentos así como la variación alélica de las poblaciones susceptibles.
Ejemplos de reacción adversa a drogas.-
Abacavir
Es una droga análoga a la guanosina que inhibe la enzima transcriptasa reversa del HIV-1 y se usa como terapia complementaria para el tratamiento de la infección HIV-1.
Se ha reportado entre un 5 y 8% de reacciones de hipersensibilidad a esta droga en las primeras 6 semanas de tratamiento. Caracterizadas por malestar, fiebre y síntomas gastrointestinales y respiratorios.
En el 2002 se reportó una fuerte asociación de la clase HLA I HLA-B*57:01 y el síndrome de hipersensibilidad al abacavir. Estudios clínicos han confirmado la base inmunológica de este síndrome. Se realizaron protocolos clínicos PREDICT-1 que mostró la iniciación de casos clínicos en pacientes con pruebas de parche positivas a la droga que confirmaron la presencia de sensibilización y ocurrieron entre 1,5 días y 3 semanas después de iniciado el tratamiento con la droga. Otro protocolo clínico el denominado SHAPE mostró que la exclusión de individuos positivos para HLA-B*57:01 eliminó la incidencia del síndrome de hipersensibilidad al abacavir en un valor predictivo negativo de 100% y un valor predictivo positivo de 55%.
Otros estudios in vitro de células de pacientes con hipersensibilidad al abacavir han demostrado la posibilidad de una activación celular al estimularlas con la droga en cultivos.
Se ha demostrado la positividad de pruebas de parche con abacavir en pacientes HLA-B*57:01 esta prueba ha resultado negativa en pacientes con otros alelos relacionados.
Carbamazepina.-
Una amina aromática anticonvulsivante usada en la epilepsia, desordenes bipolares y neuralgia del trigémino. El espectro de reacciones adversas a estas drogas mediadas inmunológicamente incluye síndrome de S/J, TEN, exantema maculo-papular, y DRESS. Se demostró en el 2004 que los individuos con el alelo HLA-B*15:02 se asociaban con la producción de síndromes de hipersensibilidad a esta droga en poblaciones de algunas regiones de China, de Tailandia, de Malasia y de la India.
Alopurinol.-
Es un inhibidor de la xantina oxidasa usada para tratar hiperuricemia y la producción de reacciones adversas con esta droga son principalmente del tipo cutáneo en aproximadamente el 2% de los individuos en tratamiento. En el 2005 se demostró la asociación con el alelo HLA-B*58:01. Se asocia con DRESS, S/J y TEN en algunas poblaciones. En el caso de alopurinol no solo la droga produjo respuesta inmune adversa sino también su metabolito oxypurinol.
Implicaciones para la práctica clínica y futuras líneas de investigación.-
La oportunidad de identificar pacientes que están en riesgo de sufrir una reacción adversa a drogas a través del estudio farmacogenético antes de administrar la droga es un concepto atractivo dado el costo, la morbilidad y la mortalidad asociadas a las reacciones adversas a drogas las cuales pudieran disminuir significativamente la incidencia de estas reacciones. Igualmente es importante destacar que la realización de pruebas de parche con medicamentos es otra herramienta accesible para decidir o no la utilización de algunas drogas causantes de reacciones adversas.
Después de los estudios PREDICT-1 y SHAPE en el año 2008, la FDA y otras organizaciones han recomendado realizar el genotipo HLA-B*57:01 a cualquier paciente que se piense tratar con abacavir y excluir del tratamiento a los pacientes positivos.
Similarmente pacientes principalmente asiáticos positivos para HLA-B*15:02 deben excluirse del tratamiento con carbamazepina.
Antes de iniciar alopurinol debe realizarse el genotipo HLA-B*58:01 y excluirse del tratamiento a pacientes positivos.
Estos ejemplos comparten hechos que demuestran la traslación de la ciencia básica a la práctica clínica y son ejemplos muy claros de medicina traslacional.
Sin embargo, los valores tan bajos predictivos positivos para las reacciones adversas a drogas asociados al genotipo HLA implica también negar el tratamiento a un número importante de pacientes que cargan el haplotipo de riesgo y que podrían tolerar la droga y ser beneficiados por ella. Por ejemplo, el valor predictivo positivo para alopurinol es solo 3%. Aunque el valor predictivo positivo para el abacavir es 55% un poco más alto.
Deberían entonces, realizarse también otro tipo de pruebas tales como reacciones cruzadas para células T. Actualmente existen avances tecnológicos para determinar el repertorio del TCR en un individuo, estudiando los genes de las cadenas variables del TCR y estudios ultrasensibles de PCR para detectar y cuantificar variantes raras del TCR. Métodos computacionales y experimentales para identificar los epítopes de HLA que producen las reacciones cruzadas patogénicas de los TCRs. Con estas pruebas podremos conocer con más detalle la inmunidad heteróloga como un mecanismo de hipersensibilidad a las drogas.
Conclusiones.-
Ciertas reacciones adversas a drogas están fuertemente asociadas con variación en los genes de HLA y las manifestaciones clínicas.
Existen modelos que explican como un compuesto molecular farmacológico puede interactuar con proteínas del MHC, tales como el modelo hapteno/prohapteno, el modelo p-i y el modelo del repertorio del péptido alterado.
Muchas asociaciones entre las reacciones adversas a drogas y los alelos HLA I y II se caracterizan por un alto valor predictivo negativo. Este hecho permite determinar el alelo asociado con el riesgo y la exclusión para el tratamiento de los individuos positivos y así eliminar estas reacciones en las poblaciones susceptibles.
El bajo valor predictivo positivo para las asociaciones entre alelos HLA y las reacciones adversas, significa que existen otros factores desconocidos hasta ahora para que las reacciones adversas a drogas mediadas por células T se produzcan.
Todavía no existe explicación para el bajo valor predictivo positivo de la asociación con el alelo HLA, la especificidad celular, el corto período de latencia que se puede observar en estas reacciones adversas a medicamentos y la persistencia en el tiempo de sensibilización a la droga, aún en la ausencia de la exposición al antígeno
Bibliografía
White KD y col., Evolving models of the immunopathogenesis of T cell-mediated drug allergy: the role of host, pathogens, and drug response. J Allergy Clinical Immunol 2015; 136(2): 219-234
Pavlos R y col., T cell mediated hypersensitivity reactions to drugs Amnu Rev Medicine 2015 66: 439-54
Naisbit D J y col., Antigenicity and immunogenicity of sulfametoxasol: demonstration of metabolism-dependent haptenation and T cell proliferation in vivo. Br J Pharmacology 2001; 133: 295-305
Pichler WJ y col., Pharmacological interactions with immune receptors: the p-i concept Allergol Int 2006; 55:17-25
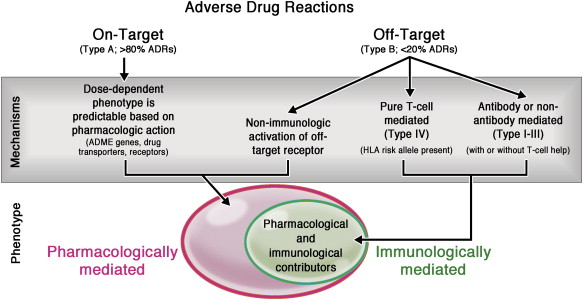
*Figura 1
Reacciones Adversas a Drogas pueden resultar de interacciones entre drogas y componentes celulares que pueden producirse tanto en el receptor blanco como fuera de él.
Variaciones en los procesos celulares que modulan absorción, distribución, metabolismo y excreción pueden inducir reacciones adversas a drogas. Transportadores de drogas y expresión del receptor blanco contribuyen a reacciones adversas mediadas principalmente por mecanismos farmacológicos (óvalo rosado). Los efectos adversos fuera del receptor blanco pueden ocurrir por mecanismos inmunológicos o no inmunológicos (óvalo verde). Los mecanismos inmunológicos incluyen tanto mediados por anticuerpos (reacciones tipo I, II y III) y mediadas por células T (reacción tipo IV).
Tomado de White K D et al J Allergy Clinical Immunol 2015
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
