Uno de los avances recientes más importantes en oncología cutánea ha sido el desarrollo y uso de vismodegib para tratamiento de carcinoma basocelular (CBC) avanzado y/o metastásico. Los estudios publicados han demostrado una respuesta clínica de hasta 55%. El medicamento actúa inhibiendo la vía del Hedgehog, la cual está muy activa en carcinomas basocelulares con mutaciones activantes en los genes Ptch1 y SMO. En el estudio clínico más grande, se utilizó vismodegib para tratar 104 pacientes con carcinoma basocelular. Se observó una respuesta parcial en 30% de los pacientes con carcinoma basocelular metastásico, y 43% en aquellos con carcinoma basocelular avanzado.
El vismodegib es altamente teratogénico y puede también causar muerte fetal, por lo que debe usarse con precaución extrema en mujeres en edad reproductiva. La dosis efectiva de vismodegib es 150 mg/ día. Las dosis de 150 mg de 1 a 3 veces por semana no han sido efectivas. Los efectos secundarios más comunes son espasmos musculares, alteración/ pérdida del sentido del gusto, disminución del apetito, estreñimiento, nausea, vómito, diarrea, cansancio, pérdida de cabello, y pérdida de peso. Estos efectos adversos llegan a ser intolerables hasta en 30 % de los pacientes.
Las indicaciones actuales para uso de vismodegib son: CBC metastásico y CBC avanzado. Aunque la definición de CBC metastásico es clara, la de CBC “avanzado” no lo es. De hecho, creo que no se cuenta con ninguna definición. Actualmente en EU se usa para tumores recurrentes, de gran tamaño, fijos a estructuras/ tejidos profundos, que abarcan múltiples unidades cosméticas, etc. Lamentablemente, también se ha empezado a abusar de su uso, aplicándolo en cualquier paciente que no quiera tratamiento quirúrgico o con radiación, o con tumores múltiples, aún cuando ninguno de ellos sea “avanzado”. Los aspectos éticos y de costo-efectividad de éstas conductas pueden ser motivo para otros comentarios o editoriales. Por el momento, quiero concentrarme en las limitaciones terapéuticas del vismodegib.
La literatura muestra respuestas entre 30-43% de pacientes tratados. Algunas de éstas respuestas son parciales y temporales. Esto significa que la mayoría de pacientes (57-70%) no responden al vismodegib. Esta falta de respuesta debe enfatizarse para que los dermatólogos puedan poner en perspectiva su uso. A continuación, presento casos en los que el vismodegib fué muy efectivo y otros en los que el no ha funcionado. Concluiré con un comentario breve sobre algunas de las posibles razones para su falta de efectividad.
Caso #1
Paciente masculino de 82 años de edad con CBC avanzado. Tenía historia de enf. pulmonar severa, diabetes descontrolada, cardiopatía isquémica y uso de anticoagulantes orales potentes. Se consideró como mal candidato para cirugía y no tenía fácil acceso a radioterapia. Se trató con vismodegib 150 mg/día con respuesta evidente a los 2 meses y total a los 7 meses. Una biopsia del tejido redundante final no mostró evidencia de CBC
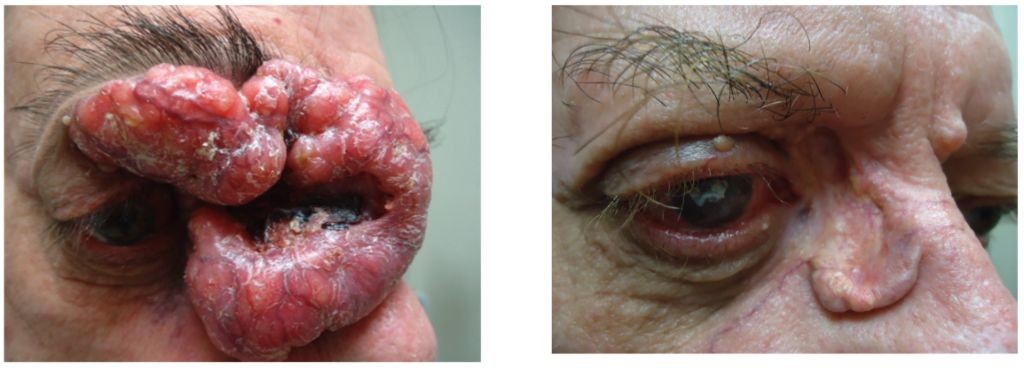
Caso #2.
Paciente masculino de 65 años de edad sin seguro médico y con CBC recurrente. El tumor estaba fijo a estructuras profundas. La tomografía computarizada no mostró compromiso óseo. Se recomendó tratamiento quirúrgico con c. de Mohs pero el paciente era muy nerviosos y se consideró incapaz de tolerar un procedimiento bajo anestesia local. Por motivos económicos, el paciente rechazó la cirugía convencional bajo anestesia general y radioterapia, prefiriendo explorar la posibilidad de tratamiento oral con vismodegib. La companía farmacéutica Genentech proporcionó el medicamento a costo mínimo y el paciente fué tratado con vismodegib 150 mg/día. Se observó respuesta parcial a los 2 meses, y completa a los 6 meses.
Caso #3
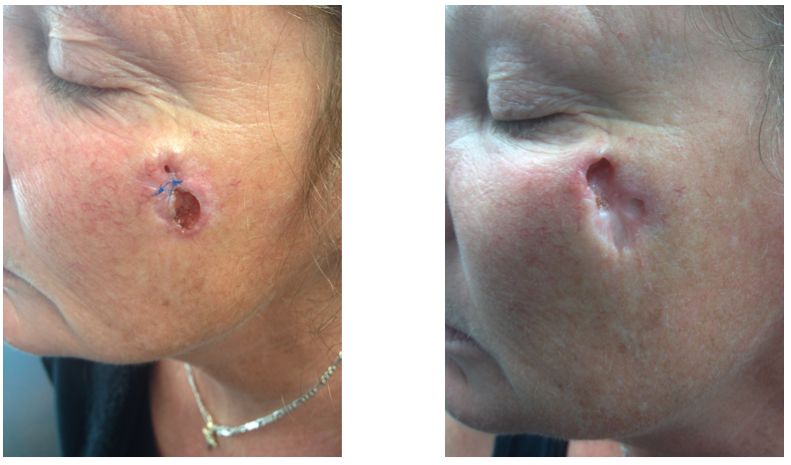
Paciente femenino de 61 años de edad, sana, con CBC avanzado. La lesión estaba fija a tejidos profundos y una tomografía computarizada demostraba afección ósea malar leve. La paciente rechazó la cirugía por temor a mutilación, y era muy jóven para tratamiento con radioterapia. Se decidió tratar con vismodegib 150 mg/día. Observándose una respuesta mínima a las 2 meses, pero sin mejoría a los 9 meses de tratamiento.
Caso #4
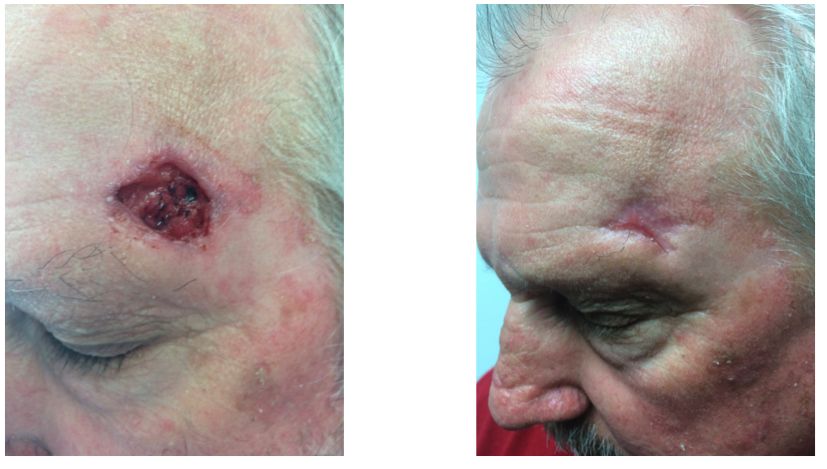
Paciente femenino de 74 años de edad, sana, con CBC recurrente. El tumor había sido tratado através de los años con 4 cirugías y un curso de radioterapia (20 sesiones). La lesión estaba fija a planos profundos. La tomografia computarizada no demostró compromiso óseo. Se inició tratamiento con vismodegib 150 mg/día. Hubo una respuesta parcial evidente a los 2 meses pero no hubo ninguna mejoría adicional durante los próximos 4 meses.
Caso #5
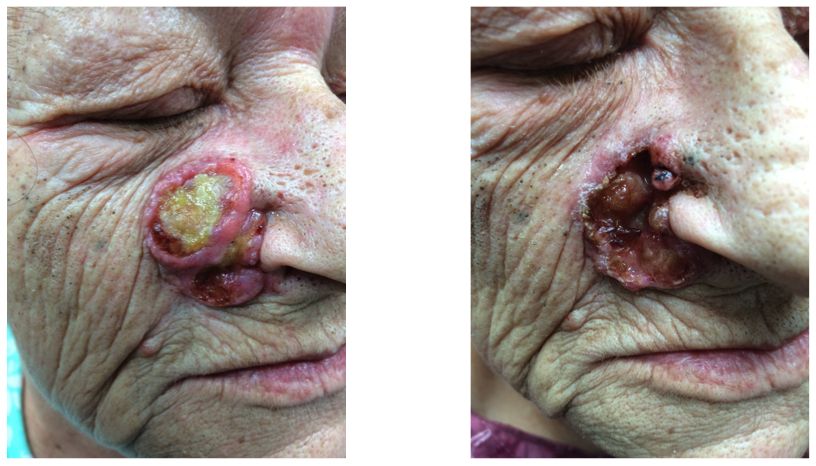
Paciente masculino de 70 años de edad con CBC recurrente múltiple. Através de los años, había sido tratado con cirugía x 3 y radioterapia x1. La tomografía computarizada demostraba gran afección ósea fronto-temporal sin afección cerebral. El paciente estaba consciente y recibió tratamiento con vismodegib 150 mg/día por 5 meses. No hubo ninguna respuesta clínica y el paciente se deterioró progresivamente hasta entrar en coma
Discusión
El descubrimiento de mutaciones en el gen PTCH1 en el síndrome de Gorlin constituyó un gran paso para el entendimiento the los mecanismos moleculares involucrados en el CBC. Las mutaciones en PTCH1, SMO, y SUFU se encuentran en más del 90% de CBCs adquiridos, y enfatizan la importancia de la vía Hedgehog (Hh) en su desarrollo. Aunque la mayoría de los CBCs puede tratarse efectivamente con cirugía o radiación, el manejo de CBC avanzado o metastásico es más complicado y menos efectivo.
El vismodegib fué el primer inhibidor de la vía Hh aprobado para tratar éstos tumores. Aunque una proporción importante de pacientes responden al medicamento, hay muchos que no lo hacen o que desarrollan resistencia. Además, los efectos adversos llegan a ser intolerables hasta en 30% de los pacientes.
Estudios recientes demuestran que los tumores resistentes desarrollan re-activación del Hh, principalmente por medio de mutaciones secundarias en SMO, SUFU, y GLI2. Estas mutaciones impiden la unión del medicamento o reactivan SMO a varios niveles. Por ejemplo, la mutación SMO (G497W) provoca un reajuste conformacional con obstrucción parcial de la entrada de la proteína-medicamento. La mutación SMO (D473Y) cambia la geometría del sitio de unión de manera que provoca ruptura de los enlaces de hidrógeno estabilizadores.
Finalmente, se postula que el CBC muestra heterogeneidad de mutaciones en diferentes partes del tumor, lo que dificulta el tratamiento con un solo inhibidor.
Podemos concluír que aunque el vismodegib es definitivamente un gran avance en el tratamiento del CBC, el medicamento tiene limitaciones importantes como gran frecuencia de efectos adversos intolerables (30%) y el desarrollo de quimio-resistencia.
Referencias
Calzavara Pinton P, Licitra L, Peris K, et al. Vismodegib in the treatment of basal cell carcinoma: indications for clinical practice. Future Oncol. 2015;11(9):1429-35.
Meani RE, Lim SW, Chang AL, Kelly JW. Emergence of chemoresistance in a metastatic basal cell carcinoma patient after complete response to hedgehog pathway inhibitor vismodegib (GDC-0449). Australas J Dermatol. 2014 Aug;55(3):218-21
Pricl S, Cortelazzi B, Dal Col V, Marson D, et al. Smoothened (SMO) receptor mutations dictate resistance to vismodegib in basal cell carcinoma. Mol Oncol. 2015 Feb;9(2):389-97.
Sekulic A, Migden MR, Lewis K, et al. Pivotal ERIVANCE basal cell carcinoma (BCC) study: 12-month update of efficacy and safety of vismodegib in advanced BCC. J Am Acad Dermatol. 2015 Jun;72(6):1021-6
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998

Gracias Dr. García. Interesante y muy útil documento que pone en perspectiva al Vismodegib porque, como usted menciona, ya se estan cometiendo abusos. Que es un gran avance no hay duda, pero aún queda mucho camino por recorrer. Sólo que toca recorrerlo con mesura.
Importante artículo sobre Vismodegib, del Dr. García Remenyería , coincido en la importancia de conocer límites y alcances del medicamento, evitar el uso indiscriminado y definir y dejar claro cuales son los carcinomas baso celulares «avanzados» ya que se puede interpretar subjetivamente .