Edición genética en kinetoplastidas
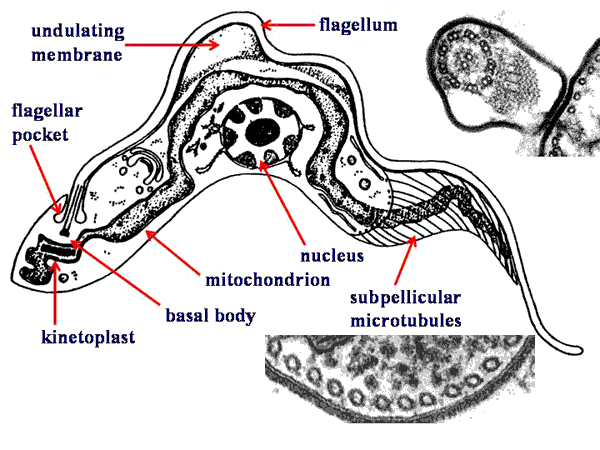
Un grupo de protozoos parásitos flagelados del orden Kinetoplastida son causantes de enfermedades en humanos con un grau impacto en salud pública; representativos de ellos tenemos a Trypanosoma brucei que produce la tripanosomiasis africana (HAT) o enfermedad del sueño, T. cruzi que produce la enfermedad de Chagas (ECh) y distintas especies de Leishmania spp. que producen la leishmaniasis [cutánea (CL), mucocútanea (MCL) y visceral (VL)]. Estas enfermedades son reconocidas como enfermedades tropicales desatendidas (Neglected Tropical Disease, NTD: siglas en inglés) por la Organización Mundial de la Salud.
Actualmente, existe un gran interés por explorar nuevos enfoques tanto de diagnóstico temprano, como el tratamiento de estas enfermedades, ya que las terapias farmacológicas de las mismas son limitadas y hay un incremento de la resistencia a muchas de las drogas utilizadas, producto de la variabilidad genética de estos organismos; esto pone en evidencia la necesidad de identificar nuevos blancos terapéuticos al igual que la evaluación de nuevas drogas. Aunque los estudios genómicos y epidemiológicos utilizando aproximaciones de geo-referencia han sido de gran importancia en el conocimiento de parásitos y vectores relacionados con estas enfermedades, la erradicación y control de las mismas requiere de fondos para generar nuevas aproximaciones en la investigación de nuevos medicamentos y potenciales vacunas.1
En la era post-genómica, la edición genética a través de la implementación del sistema CRISPR-Cas (Clustered Regularly Interspaced Short Palindromic Repeat-associated protein; Repeticiones palindrómicas cortas interespaciadas y agrupadas regularmente), un sistema de defensa de organismos procariotas, ha llegado a ser una herramienta extraordinaria en un rango amplio de estudios que incluyen expresión genética, búsqueda y análisis de nuevos blancos de drogas, terapia genética, entre otros.2
Estudios previos muestran la implementación del sistema CRISPR-Cas en organismos kinetoplastidas, como T. cruzi y Leishmania spp., demostrando su uso eficiente en la edición del genoma de estos parásitos; es así que la edición genómica ha abierto una ventana molecular importante en el estudio funcional de proteínas, en la caracterización de las rutas metabólicas, en la validación de blancos moleculares alternativos para las intervenciones antiparasitarias y el estudio de la biología y la patogénesis de estos parásitos. Las diferentes estrategias que se han desarrollado para implementar la edición del genoma en tripanosomátidas por CRISPR / Cas9 y los factores diferenciales respecto a otros organismos eucariotes han sido previamente discutidos.3
Entre los factores que han mostrado diferencia en el proceso de edición genética entre tripanosomátidas y otros sistemas celulares, han sido los mecanismos de reparación del DNA. Previamente, se ha demostrado que el proceso de edición mediado por el sistema CRISPR requiere la formación del complejo Cas9/gRNA (RNA guía), ribonucleoproteína, que reconoce el DNA blanco generando una ruptura de la doble cadena (DSB), lleva a modificaciones en la secuencia del genoma y posterior reparación mediante los mecanismos conocidos como la unión de extremos no homólogos (NHEJ) y la reparación dirigida por homología (HDR). Una gran diferencia con otros sistemas celulares es que el sistema de reparación NHEJ está ausente en tripanosomátidas, y en su lugar utilizan el sistema HDR con gran eficiencia para inducir la reparación de DSB por recombinación homóloga en el sitio de escisión Cas9 (Lander et al.2015); un mecanismo alternativo de reparación de DSB llamado unión final mediada por micro homología (MMEJ) ha sido descrito en tripanosomátidas.3,4,5 La ausencia de NHEJ para la reparación de rotura de doble cadena en tripanosomátidas plantea limitaciones en el estudio de la interrupción de genes esenciales; sin embargo, alternativas basadas en el sistema CRISPR utilizando como blanco RNA en lugar de DNA están en evaluación.6
Esperemos en un futuro cercano, poder contar con resultados conducentes al desarrollo de mejores tratamiento y control de estas enfermedades.
Referencias
- Filardy AA, et al. (2018) Human Kinetoplastid Protozoan Infections: Where Are We Going Next? Front. Immunol. 9:1493. doi: 10.3389/fimmu.2018.01493
- Mendoza-León A. https://piel-l.org/blog/41864; b. https://piel-l.org/blog/43990; c. https://piel-l.org/blog/41487
- Lander, N., & Chiurillo, M. A. (2019). State-of-the-art CRISPR/Cas9 Technology for Genome Editing in Trypanosomatids. Journal of Eukaryotic Microbiology. doi:10.1111/jeu.12747.
- Zhang W-W, Lypaczewski P, Matlashewski G. (2017). Optimized CRISPR-Cas9 genome editing for Leishmania and its use to target a multigene family, induce chromosomal translocation, and study DNA break repair mechanisms. mSphere 2:e00340- 16. https://doi.org/10.1128/mSphere.00340-16
- Sollelis, L. et al. (2015). First efficient CRISPR-Cas9-mediated genome editing inLeishmaniaparasites. Cellular Microbiology, 17(10), 1405-1412. doi:10.1111/cmi.1245
- Konermann, S., Lotfy, P., Brideau, N. J., Oki, J., Shokhirev, M. N., & Hsu, P. D. (2018).Transcriptome Engineering with RNA-Targeting Type VI-D CRISPR Effectors. Cell, 173(3), 665–676.e14. doi:10.1016/j.cell.2018.02.033
Alexis Mendoza-León, PhD. Email: [email protected]
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
