Además de las células de Langerhans y las células dendritas dérmicas, en la piel habita otro grupo denominado células dendríticas plasmocitoides (CDp), cuya función es tema de debates y controversias.
A pesar que las CDp se encuentran en la piel normal en escasos números, algunos investigadores todavía dudan si estas células están aumentadas en procesos inflamatorios crónicos como la psoriasis.
Recientes estudios en psoriasis apoyan el papel de CDp durante la fase de iniciación del proceso inflamatorio.
En primer lugar, en experimentos de xenotrasplante con ratones inmunosuprimidos, a los cuales se le trasplantó piel no lesional de pacientes con psoriasis, se demostró que el solo estrés causado por el trasplante fue suficiente para desarrollar psoriasis de forma espontánea en el injerto. Además mostraron que el bloqueo de IFN-alfa impidió el desarrollo de psoriasis. Resultados que sugirieron la participación de CDp, ya que en los inicios de la enfermedad son estas células la principal fuente de IFN-alfa en la piel (Nestle y Nickoloff , 2005).
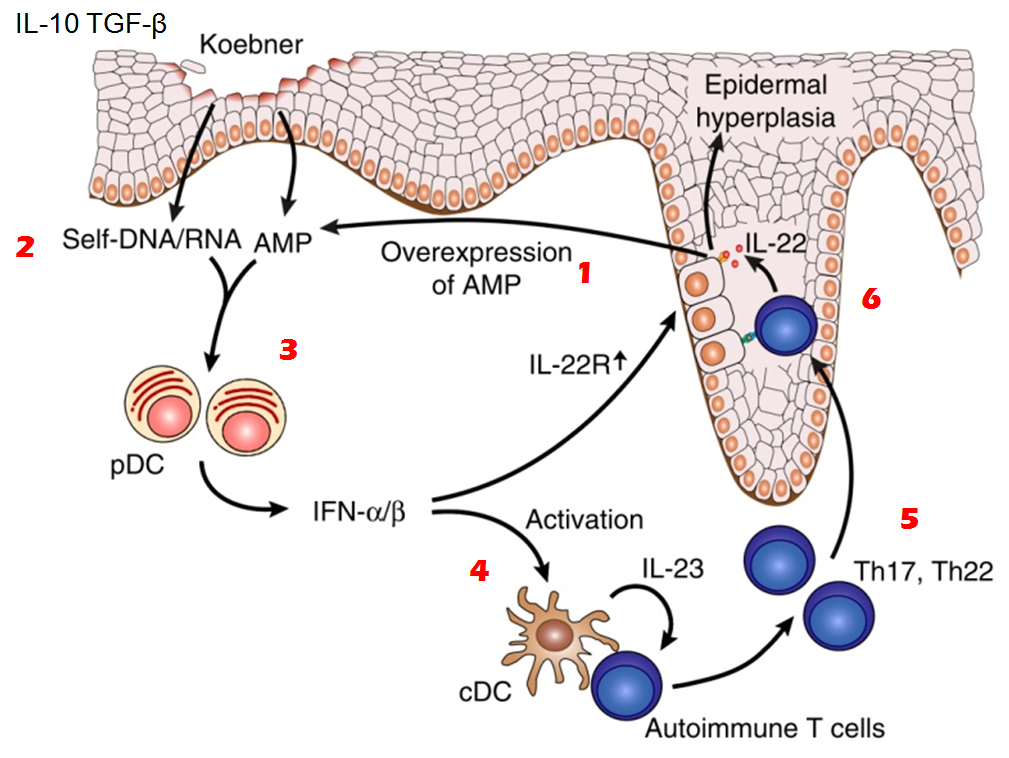
En segundo lugar, el mismo grupo de investigadores demostró que el péptido catiónico antimicrobiano LL37 está aumentado en psoriasis (Nestlé y Gilliet , 2005). Otros estudios mostraron que el LL37 forma complejos con ácidos nucleícos (ADN/ARN) extracelulares y los receptores intracelulares TLR7 y TLR9 (Lande et al., 2007). Los ácidos nucleícos nucleícos provienes de células moribundas. Los complejos promueven la activación de las CDp y la subsecuente producción de interferones tipo I (IFN-alfa e IFN-beta).
En la dermis, el IFN.alfa producido por las CDp promueve la maduración de las células dendríticas mieloides (ie. Langerhans), las cuales producen IL-23 que estimulan a linfocitos T autorreactivos capaces de migrar a la epidermis. Al reconocer un autoantígeno en los queratinocitos, estos linfocitos T autorreactivos se transforman en Th17 productoras de IL-17 e IL-22 (Nestlé y Gilliet , 2005).
El IFN-alfa puede sobrerregular la expresión en los queratinocitos del receptor de la IL-22, aumentando la capacidad de respuesta a la IL-22, la cual induce la hiperproliferación de queratinocitos, que conduce a la hiperplasia epidérmica característica de la psoriasis. Además junto con la IL-17, la IL-22 promueve la producción de más LL37, proporcionando así un circuito de retroalimentación positiva que amplifica la autoinmunidad promovida por el IFN-alfa (Conrad & Gilliet 2012).
Lo observado en psoriasis con las CDp, se puede extrapolar a otras enfermedades de la piel, y permitirían comprender los mecanismos de la inmunopatogénesis de las heridas o traumas cutáneos, como el fenómeno de Köebner.
Dermatología traslacional o lo que es lo mismo, investigación básica al servicio de la investigación clínica.
Bibliografía:
Conrad C, Gilliet M. Type I IFNs at the Interface between Cutaneous Immunity and Epidermal Remodeling. J Invest Dermatol 2012;132:1759-1762.
Lande R, Gregorio J, Facchinetti V, Chatterjee B, Wang YH, Homey B, et al. Plasmacytoid dendritic cells sense self-DNA coupled with antimicrobial peptide. Nature 2007;449:564–569.
Nestle FO, Nickoloff BJ. From classical mouse models of psoriasis to a spontaneous xenograft model featuring use of AGR mice. Ernst Schering Res Found Workshop 2005:203–212.
Nestle FO, Gilliet M. Defining upstream elements of psoriasis pathogenesis: an emerging role for interferon alpha. J Invest Dermatol 2005;125:xiv–xv.
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998

Gracias Felix por esta puesta al dia de los nuevos recovecos de la inflamacion y sobretodo de lo que tu representas para los latinoamericanos en esa investigacion basica puesta al servicio de nosotros los clinicos.
Gracias por la cita de ese gran hombre que fue Adolfo Suarez y gracias por la mancheta de Orwell el de la famosa frase «Big Brother is watching you»
Jaime Piquero Martin
Gracias Jaime por tus comentarios.La idea es siempre lograr la excelencia y poner a mover el cerebro de nuestros estudiantes y colegas.
Felix
Felix excelente articulo y muy bien resumido me interesaría me pases las referencias originales saludos