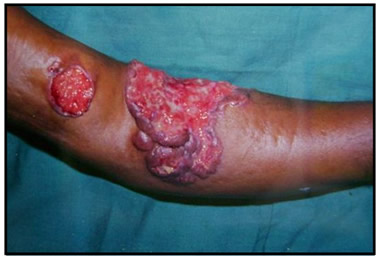
C3F1: Lesión tumoral ulcero-vegetante en antebrazo izquierdo y lesión satélite en tercio inferior de brazo izquierdo. Para entonces, el paciente no tenía compromiso ganglionar adyacente ni en otras áreas del organismo. Fue clasificado con una Enfermedad de Hodgkin de localización primaria (?) cutánea de Celularidad Mixta. Lo presenté en la XVIII Reunión Anual de la SVDCD, en la Sesión Anatomo-Clínica (1982). Me acompañaron los Drs. Arveláez F, Rondón A y León L.
C3F1: LINFOMA DE HODGKIN CUTANEO DE CELULARIDAD MIXTA. Caso presentado en la XVII Reunión Anual de la SVDCD, 1982, Sesión Anatomo- Clínica.
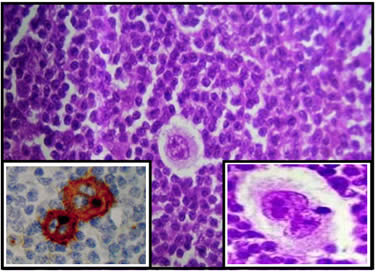
C3F2: Las fotografías histológicas son muy demostrativas: Infiltrado difuso de linfocitos pleomórficos, formando "anillos como rosetas", dando patrón nodular y difuso, presentando las clásicas células de Reed-Sternberg (HRS) caracterizadas como una célula neoplásica con abundante citoplasma, y al menos dos lóbulos nucleares con nucléolos prominentes. El inciso del ángulo inferior derecho, muestra a gran aumento HE (X 45) una célula típica de HRS, intensamente pleomórfica fagocitando un linfocito atípico. El inciso situado en el ángulo inferior izquierdo (X45) muestra la célula HRS, reactiva al antígeno CD30 (1').
C3F2: LINFOMA DE HODGKIN. CLASICA CELULA DE REED-STERNBERG. Rodeado de infiltrado linfocitario pleomórfico. HE X 16
INCISO IZQUIERDO: LINFOMA DE HODGKIN. CELULA DE REED-STERNBERG Reactivo al antígeno CD-30 (1')
INCISO DERECHO: LINFOMA DE HODGKIN. CELULA DE REED-STERNBERG HE X45
NOTA: El inciso del ángulo inferior izquierdo de la foto C3F2, que representa una reactividad de la célula HRS a CD30, fue tomado de la Figure 31-18 del trabajo de Murphy GF y Schwarting R, publicado en (1'), para complementar el aspecto inmunohistoquímico contrastado con la HE.
Este es un caso que demuestra cuán elocuente es una buena microfotografía, para demostrar todas las facetas de la histopatología y la inmunohistoquímica, que pueden ocurrir en una determinada enfermedad.
COMENTARIOS:
El Linfoma de Hodgkin (LH) hoy día constituye un grupo de condiciones linfoproliferativas, relativamente comunes, que guardan en común su frecuente origen en ganglios linfáticos cervicales, ocurrencia en adultos jóvenes, presencia de células HRS y el infiltrado pleomórfico de linfocitos-T. No obstante, hay variantes que expresan reacción antigénica del linaje de células B (CD19, CD20, CD22, etc.), mientras que el tipo clásico de LH expresa CD30 (1').
Las alteraciones histológicas en el LH con compromiso cutáneo, recuerdan a las modificaciones que ocurren en los ganglios linfáticos. Se trata de un patrón nodular o difuso con ausencia de epidermotropismo. Es probable que en realidad la EH represente todo un espectro de patrones clínico-patológicos disímiles y no que se trate de una sola enfermedad. Se piensa que el compromiso cutáneo sea secundario a la afectación ganglionar. En el Dx. diferencial hay que considerar otros tipos de linfomas: Linfoma de Células "B" grandes ricos en células "T"; Linfoma de Células "B" Grandes Difuso; Linfoma de Células "T" Anaplásico; Hiperplasia Linfoidea Reactiva (1').
Aunque la presencia de la célula de Stermberg-Reed/ células de Hodgkin, sugeriría la EH, ellas, según algunos autores, no son diagnósticas por si mismas.
El Diagnóstico de EH se establece por la definitiva identificación de la célula HRS y variantes (Células de Hodgkin), caracterizada por una célula gigante neoplásica de 12 a 40 micras en diámetro con núcleo grande y prominente. El núcleo puede ser simple o múltiple y un hallazgo característico es un núcleo en forma de semilla, dividido en dos, dando apariencia de imagen en espejo. Para el diagnóstico histológico de la enfermedad, no solo es importante la identificación de las células características de esta afección, sino el medio en que asientan: es decir, células inflamatorias no neoplásicas como son linfocitos reactivos, histiocitos (macrófagos) y granulocitos, plasmocitos y eosinófilos, dando un patrón granulomatoso. El tejido neoplásico en ésta enfermedad contiene un pequeño número de células esparcidas mononucleares grandes (células de Hodgkin) y células tumorales multinucleadas designadas HRS. Estas células tumorales están rodeadas habitualmente por una corona de linfocitos T en rosetas.
Se ha reportado transcripción genética de NPM-ALK en una sub-población de ALCL (Linfoma de Células Grandes Anaplásicas), casi exclusivamente en células T o en null-cell, y en raros casos en EH. Estos hallazgos muestran que algunos casos de EH, pueden estar estrechamente relacionados con ALCL, marcando de ésta forma nuevas hipótesis sobre su evolución biológica.
Estos hallazgos, junto con resultados inmunocitoquímicos, que muestran muchas semejanzas entre la célula grande atípica en papulosis linfomatoide (PL) tipo A y células de EH y HRS, soportan el punto de vista de que la PL tipo A y la EH son afecciones estrechamente relacionadas. Los resultados de recientes estudios indican una estrecha relación entre PL tipo B y estados tempranos de micosis fungoides.
Desórdenes linfoproliferativos primarios cutáneos CD30+, incluyendo CD30+ALCL (linfoma de células grandes anaplásicas), PL y casos borderline representan un continuum clínico-patológico, según el grupo de Kang SK, Chang SE, Choi JH et al (2002).
En un número significante de pacientes con GSS (granulomatous slack skin), la EH se puede desarrollar, de varios años a escasas décadas, después de iniciarse la dermatosis. De Gregorio R et al. reportaron el caso Nº. 20 de GSS y el Nº. 70 de GSS asociado a EH.
Aún no está clara la explicación porque la transformación de GSS en EH, ocurre mucho más frecuente que la clásica MF en EH.
5 a 20% de pacientes con PL, desarrollan "otro tipo" de linfoma, usualmente MF, ALCL o EH, bien antes de la instalación de PL, concurrente con ella o después de ella. PL parece de ésta forma estar relacionada con estas otras enfermedades, más que ser coincidente con ellas. La transformación de MF o EH en ACLC, se ha demostrado que ocurre y por analogía, EH y MF, han sido observadas en el mismo paciente.
De estas hallazgos, los autores han concluido que casos de EH clásica con células HRS derivada de células T, definitivamente existen, aunque su incidencia global en muy baja (1-2%). Aún dentro de los casos positivos con marcadores de células T, solo una minoría (15%) fueron derivados de células T. La mayoría (85%) se originaron de células B, indicando que los antígenos de células T, expresados por células HRS, en contraste con aquellos expresados por linfoma no-Hodgkin, son de un linaje no específico.
References:
(1'): Murphy G F, Schwarting R. Cutaneous Lymphomas and Leukemias (in) Lever´s Histopathology of the Skin (Editor-in-Chief David E. Elder; Associate Editors: Elenitsas R, Johnson, Jr. B L, Murphy G.F). Hodgkin Lymphoma, 9TH edition, 2005.pages 948-950
Las Referencias Nº- 1-15, fueron tomadas de: Dermatopathology: Practical & Conceptual. January- March, 2007. Volume 13, #1, http://www.derm101.com
1. Rosai J. Lymph nodes. In: Rosai J, ed. Ackerman's Surgical Pathology. 8th ed. St. Louis: Mosby, 1996: 1966-1970.
2. Weiss LM, Arber DA, Chang KL. Lymph nodes and spleen. In: Silverberg S, ed. Principles and Practice of Surgical Pathology and Cytopathology. 3rd ed. Singapore: Churchill Livingston, 1997:706.
3. Hodgkin T. On some morbid appearances of the absorbent glands and the spleen. Medical Chirurgical Transactions 1832; 17: 68-114.
4. Sternberg C. Uber eine eigenartige unter dem Bilde der Pseudoleukamie verlaufende Tuberculose des lymphatischen Apparates. Ztschr Heilk 1898; 19:21-90.
5. Aster J. Diseases of white blood cells, lymph nodes, spleen and thymus. In: Kumar V, ed. Robbins and Cotran Pathologic Basis of Disease. 7th ed. Philadelphia: Elsevier Saunders, 2005:686.
6. Stein H. Hodgkin lymphoma. In: Jaffe E, ed. WHO Classification of Tumours, Pathology and Genetics, Tumours of Haematopoietic and Lymphoid Tissue. Lyon: IARC, 2001:239.
7. Yee HT, Ponzoni M, Merson A, et al. Molecular characterization of the (2; 5) (p23; q35) translocation in anaplastic large cell lymphoma (Ki-1) and Hodgkin's disease. Blood 1996; 3:1081-1088.
8. Willemze R, Scheffer E, Van Vloten WA, Meijer CJ. Lymphomatoid papulosis and Hodgkin's disease: are they related? Arch Dermatol Res 1983; 3:159-167.
9. Bustos de Abajo M, Serrano Ortega S, Medina Cano MT. Lymphomatoid papulosis evolving into malignant lymphoma. Clinico-pathological and immunohistochemical study of 3 cases. Med Clin (Barc) 1993; 6: 220-222.
10. Cohen PL, Butmarc J, Kadin ME. Expression of Hodgkin's disease associated antigen BLA.36 in anaplastic large cell lymphomas and lymphomatoid papulosis primarily of T-cell origin. Am J Clin Pathol 1995; 1:50-53.
11. Kang SK, Chang SE, Choi JH. Coexistence of CD30-positive anaplastic large cell lymphoma and mycosis fungoides. Clin Exp Dermatol 2002; 3:212-215.
12. DeGregorio R, Fenske NA, Glass LF. Granulomatous slack skin: a possible precursor of Hodgkin's disease. J Am Acad Dermatol 1995;6: 1044-1047.
13. Matthias F. Observations about mycosis fungoides, lymphomatoides papulosis, anaplastic large-cell lymphoma, and Hodgkin's disease-and interferences from them. Dermatopathology: Practical & Conceptual 2000; 6(4). Available at: www.derm101.com.
14. Seitz V, Hummel M, Marafioti T, Anagnostopoulos I, Assaf C, Stein H. Detection of clonal T-cell receptor gamma-chain gene rearrangements in Reed-Sternberg cells of classic Hodgkin disease. Blood 2000; 10:3020-3024.
15. Davis TH, Morton CC, Miller-Cassman R, Balk SP, Kadin ME. N Engl J Med 1992; 17:1115-1122.
| CASO Nº 3-A CASO ANEXO DRA. RAMOS.doc 1573K Descargar documento |
 PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998
PIEL-L Latinoamericana Publicacion periodica en dermatologia | Fundada en 1998

Estimado Dr Planas, su caso aunque hiperpatético clínicamente, me recuerda un caso que yo presenté, de un linfoma de Hodgkin, que llegó a mi consulta, con una clínica de inflamción localizada en el cuello (sitio previo de biopsia donde diagnosticaron por primera vez el linfoma), y yo me plantee algunos diagnósticos y al hacer la biopsia la patologia había infiltrado piel. Conservo el caso y recuerdo que en la revisión de la literatura, alguien decía que había más clasificaciones de linfomas que patólogos mismos. Le envío la foto clínica y las histológicas, y algunos slides teóricos para ver si ud las puede publicar en su sesión. Saludos.
Dra Raquel M Ramos M
Apreciada Raquel: Recibí tu interesante caso de Enfermedad de Hogkin Cutánea, en el cual ya estoy trabajano (editando) y al cual le agregaré un pequeño comentario. Tenemos que resolver un pequeño problema previo con los Editores, en el sentido de que no se publicó la versión definitiva del Enfermedad de Hodgkin y estoy esperando por ella. Una vez concluido tu caso, que probablemente lo tenga listo en dos(2)días, se lo envío a Rolando, encargado de la ediciones impares del Blog, para que lo analice con Jaime y aprueben su publicación. Por mi parte tiene luz verde porque está muy bien implementado y con buenas fotos. Agradecido por tu colaboración.
Dr. Guillermo Planas Girón
Ccs-Venezuela
Agradecido a Rolando y a José Hernández, por haber publicado, la «versión definitiva» sobre Enfermedad de Hodgkin. Esos pequeños errores son explicables por la numerosa información recibida y acumulada y por supuesto que tienen que manejar. Es el precio, que ocasionalmente, tenemos que pagar por el crecimiento. Pero hay que seguir adelante.
Un saludo Cordial
Guillermo Planas G.